No segundo artigo da série sobre interações moleculares, vamos ver um experimento que usa materiais muito simples mas que mostra um fenômeno intrigante e inesperado.
Para entender o que acontece no vídeo, temos de observar cada parte com cuidado e pensar nas interações que ocorrem em cada caso. Temos de considerar como as moléculas de água interagem entre si e com a placa de vidro. Da mesma forma, vamos pensar no que ocorre com as moléculas do etanol e sua interação com o vidro. Por fim veremos porque a água e o etanol se comportam da forma observada no experimento.
Este experimento foi descrito como uma demonstração para o retroprojetor em um artigo no Journal of Chemical Education (https://pubs.acs.org/doi/pdf/10.1021/ed070p253). escrito por Todd Silverstein em 1993.
Água e vidro
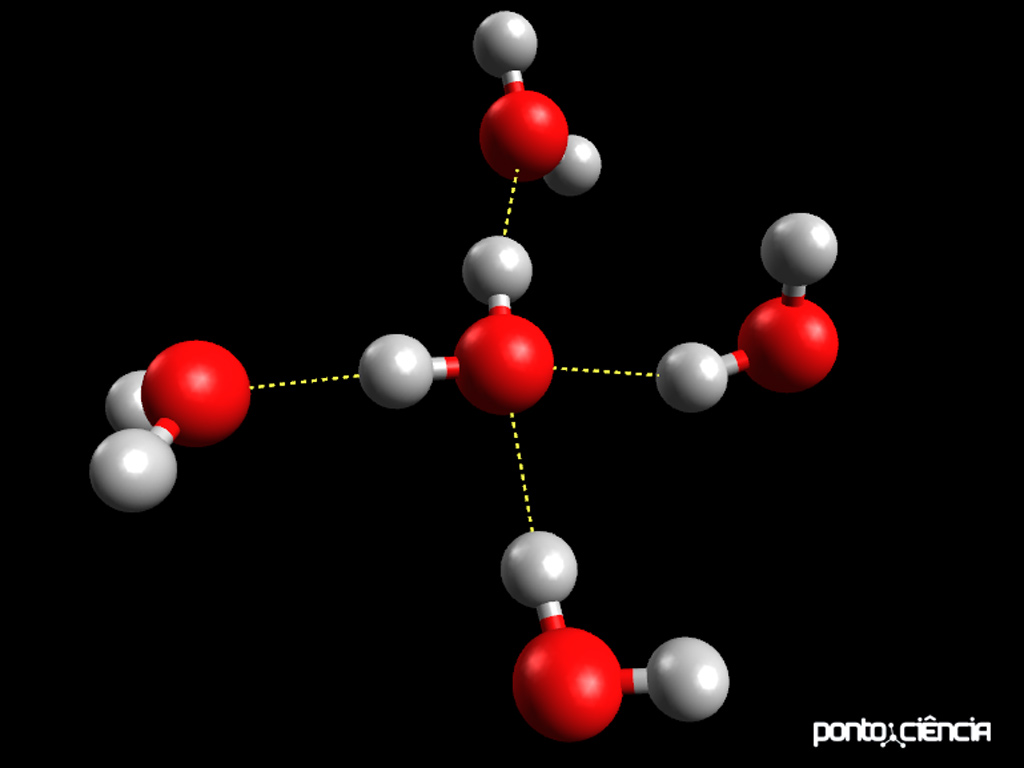
As moléculas de água possuem uma geometria angular, que as torna polares. A grande diferença de eletronegatividade entre os átomos de oxigênio e hidrogênio faz com que as interações entre o hidrogênio de uma molécula e o oxigênio de outra sejam tão fortes que elas são classificadas como “ligações de hidrogênio”, um caso especial entre as interações dipolo-dipolo. Uma molécula de água pode formar até quatro ligações de hidrogênio com moléculas vizinhas, como podemos ver na imagem abaixo.
A intensidade dessas interações é responsável por diversas propriedades especiais da água. A água líquida tem uma temperatura de ebulição muito maior que o esperado para uma molécula tão pequena e leve. A alta tensão superficial da água é outra consequência da intensidade dessas interações.
Quando colocamos uma gota de água em uma superfície em que ela não faz boas interações, percebemos que a gota fica arredondada, quase uma esfera. Foi o que vimos no artigo anterior, em que colocamos gotas de água na areia mágica – Investigando a areia mágica – Interações em microescala 1.
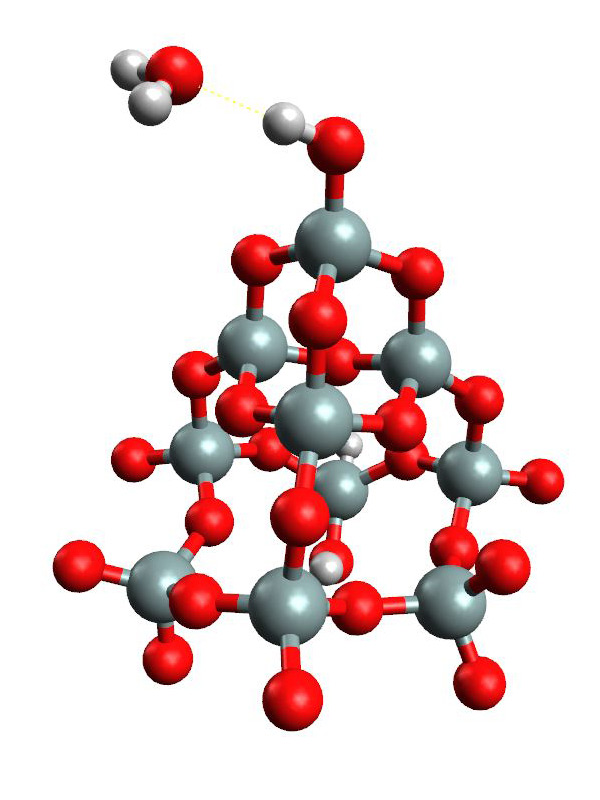
Já na placa de vidro, a gota de água fica ligeiramente arredondada, mas observamos que a água molha sim o vidro. Na superfície do vidro temos grupos Si-OH e Si=O que podem fazer ligações de hidrogênio com a água (veja a segunda figura abaixo).
Álcool e vidro
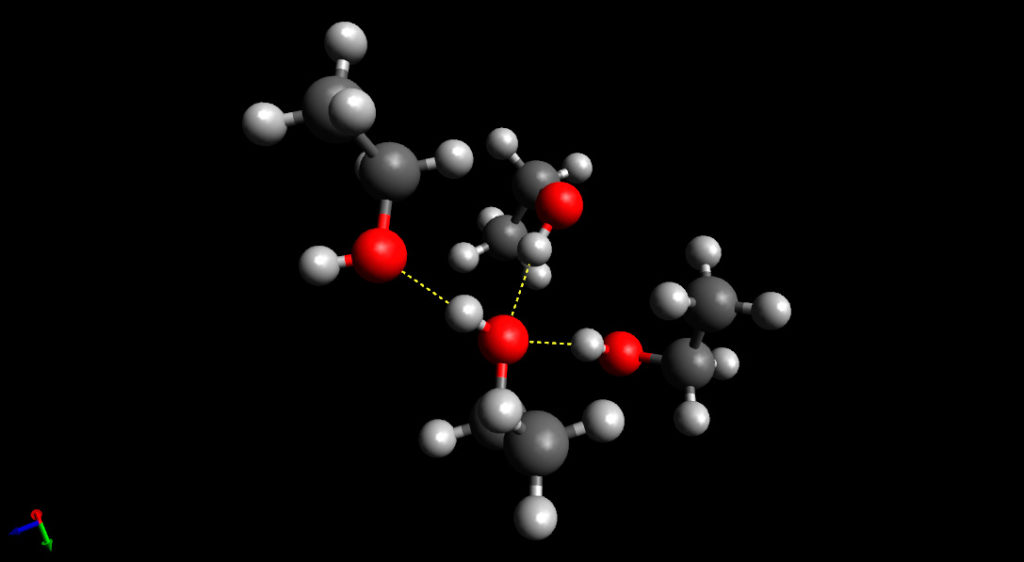
Quando comparamos o comportamento da gota de álcool no vidro, podemos ver que o líquido se espalha muito mais, não formando gotas arredondadas. As moléculas de álcool etílico possuem um grupo -OH que pode formar ligações de hidrogênio com moléculas vizinhas. Na imagem abaixo vemos que uma molécula de etanol central pode interagir com até 3 outras. As interações entre as moléculas de etanol são mais fracas que entre as moléculas de água.
O álcool etílico consegue interagir bem com o vidro, como a água. Ele se espalha mais porque as forças internas na gota de álcool são mais fracas do que no caso da água.
Por que a gota foge?
Se você colocar água e álcool em um mesmo recipiente, verá que os líquidos são perfeitamente miscíveis em qualquer proporção. Ou seja, sempre conseguimos dissolver o álcool na água e vice-versa.
Mas, então porque a gota de álcool não se dissolveu na água?
Quando a gota de álcool encosta na gota de água, as moléculas de água ficam entre a opção de formar interações com o álcool ou continuar com as interações com moléculas de água. Se você colocar os dois líquidos em um copo e misturar, você não está dando nenhuma opção – eles vão misturar e pronto. Mas, sabendo que as interações entre as moléculas de água são mais fortes, é mais fácil entender porque a gota se afasta e se mantém com apenas água.
De acordo com o autor do artigo citado acima, “A alta tensão superficial da água cria uma barreira cinética para a mistura das duas gotas. Muito antes das duas gotas terem a chance de se misturarem, a gota de água se move ao longo da placa, se afastando da gota de etanol”.
Investigando outras gotas
Você pode investigar com os seus alunos o que aconteceria com outros líquidos. Álcool iso-propílico, acetona, acetato de etila são alguns dos candidatos.
Outro fator que influencia o resultado do experimento é a superfície em que ele é feito. O experimento funciona como planejado em placas de vidro comum. Usando placas de vidro borosilicato (“Pyrex”, como placas de Petri de laboratório) percebemos que as gotas se misturam imediatamente ao se encontrarem. Você pode experimentar outras superfícies ,como plásticos diversos.
Finalmentes

Se você gostou destes experimentos e da explicação, não esqueça de compartilhar a postagem com colegas e amigos. Ficou com dúvida ou teve uma ideia brilhante? Deixe seu comentário abaixo.

