O que é uma pilha “humana”? É uma pilha em que você faz parte do circuito! Para conhecer melhor essa pilha em ação, veja o vídeo abaixo, e depois, siga lendo para entender como ela funciona.
Faça o seu
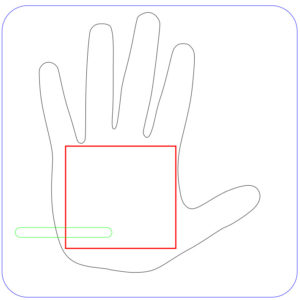
Para montar a pilha, nós cortamos dois quadrados de MDF de 6 mm de espessura no corte a laser. Ao mesmo tempo em que fizemos o corte, também fizemos a gravação das placas, desenhando o contorno de uma mão e um quadrado onde encaixaremos as placas metálicas. Nós experimentamos com a potência e a velocidade do laser de modo a rebaixar o MDF exatamente o suficiente para que as placas de cobre e de zinco ficassem encaixadas na mesma altura da superfície da placa de MDF.
Prendemos um fio encapado nas placas de cobre e zinco usando um parafuso, que conecta as placas com bornes de plugue banana. Ligamos um multímetro aos bornes usando cabos com plugues do tipo banana.
Como usar na sua aula e o que acontece
Finalmentes
Pilhas e baterias são responsáveis por podermos ter aparelhos portáteis como telefones celulares, rádios, lanternas e calculadoras. Você costuma fazer experimentos com pilhas com seus alunos? Discute as questões ambientais relacionadas com o seu descarte? Gostou do nosso experimento? Juntamos mais experimentos com pilhas neste artigo do XCiência. Comente abaixo e compartilhe com seus colegas.

