Experimentos que apresentam resultados inesperados são, em geral, experimentos que chamam muito a atenção e demandam uma explicação. Neste artigo apresentamos um experimento ao mesmo tempo muito simples (em termos dos materiais usados) e surpreendente.
Preparando o experimento
Você vai precisar de:
- água com corante alimentício;
- álcool etílico 92o GL com um outro corante alimentício de cor diferente da água;
- uma placa de vidro comum.
Vai precisar também dois conta-gotas para pingar os líquidos e de uma folha de papel branco que deve ser colocada abaixo da placa de vidro e ajuda na visualização. O experimento está pronto para a aula. Você pode realizar este experimento como uma demonstração (em que apenas o professor manipula os materiais enquanto dialoga com os alunos) ou como um experimento em que os alunos irão manipular os reagentes. Caso os alunos façam o experimento, separe-os em grupos e prepare um conjunto de placa de vidro e frascos com água e álcool para cada grupo.

Realizando o experimento
Inicialmente, peça para os alunos fazerem uma previsão: o que acontece quando pingamos algumas gotas de água sobre o vidro: ela irá se espalhar completamente, molhando o vidro, ou irá permanecer junta no local onde você pingar? Após a previsão dos alunos, pingue a água com corante sobre a placa. Chame a atenção dos estudantes para o fato de que as gotas e água permaneceram juntas e possuem uma superfície arredondada.
Repita o processo de pedir uma previsão e pingar o líquido na placa de vidro, mas agora para o álcool etílico. O álcool etílico irá se espalhar mais ou menos do que a água? Quando pingamos o álcool no vidro percebemos que ele se espalha por uma área muito maior que no caso da água e não conseguimos ver uma superfície arredondada.
Por fim, peça aos alunos que façam uma previsão sobre o que aconteceria se você pingasse o álcool próximo da gota de água. de modo que ele se espalhasse e tocasse a gota de água. Será que o álcool irá se misturar com a água?
Considerando que os estudantes sabem que o álcool etílico é solúvel em água, é muito comum que eles respondam que sim, o álcool e a água irão se misturar. Veja no vídeo abaixo o que acontece.
O que acontece
Quando pingamos uma gota de água na placa de vidro, podemos notar que, por uma lado, a gota se espalha um pouco, molhando a placa de vidro, e por outro, que a gota apresenta uma superfície arredondada.
A água não se espalha completamente pela superfície do vidro porque as forças de atração entre as moléculas de água superam a sua atração pela superfície do vidro. A superfície do vidro comum é ligeiramente polar. O principal componente do vidro é o dióxido de silício, SiO2. O dióxido de silício é um sólido covalente, em que os átomos de silício ficam no centro de um tetraedro, cercados por quatro átomos de oxigênio. Na imagem abaixo, o silício está em cinza e o oxigênio em vermelho.
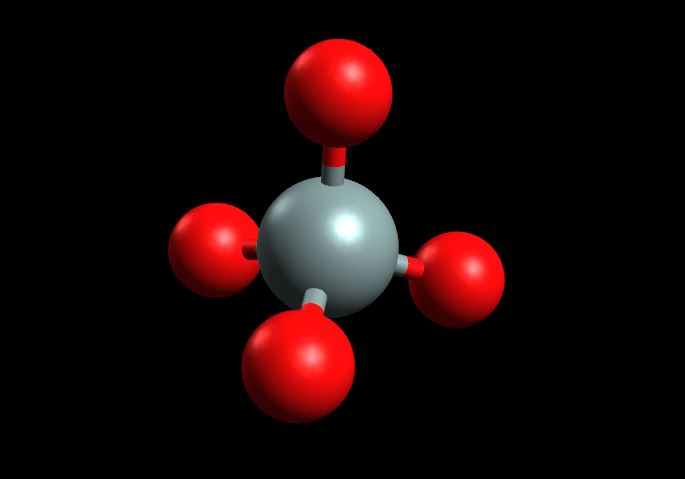
Os tetraedros se conectam e se estendem em todas as direções, mas sem formar uma estrutura ordenada, como um sólido cristalino. Por isso dizemos que o vidro é um sólido amorfo.
Na superfície do vidro podemos ter grupos Si-O-Si e também grupos Si-OH, estes últimos sendo mais polares. Podemos ver na imagem abaixo um grupo Si-OH fazendo uma ligação de hidrogênio com uma molécula de água.
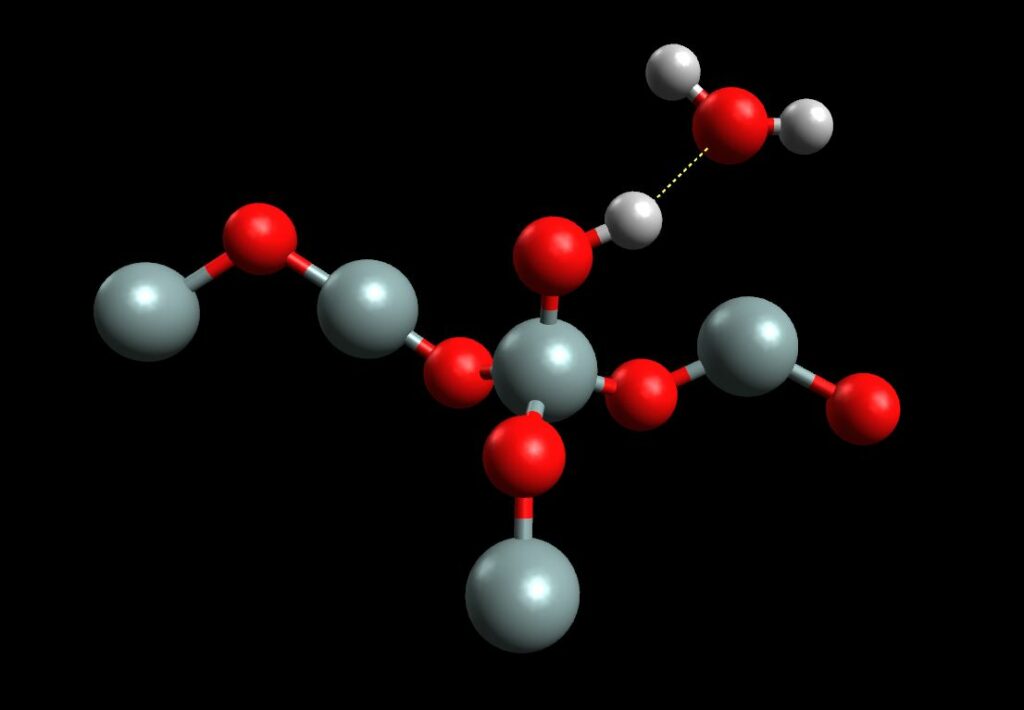
Mesmo com uma superfície levemente polar, a interação da água com o vidro não se compara com a interação da água com outras moléculas vizinhas de água. E assim a água fica coesa, em uma gota com superfície arredondada e que não se espalha muito.
Ao colocarmos o etanol no vidro, vemos que ele se espalha muito mais. O etanol é muito menos polar que a água e suas interações com moléculas vizinhas de álcool são muito mais fracas.
Assim, quando colocamos uma gota de álcool etílico próxima da gota de água, o álcool se espalha e encosta na água. Neste momento, duas coisas poderiam acontecer: os dois líquidos poderiam se misturar… ou eles podem se separar, com a gota de água literalmente fugindo do álcool.
Apesar do álcool e da água serem totalmente miscíveis quando colocados em um mesmo copo, aqui podemos ver que para a água, entre fazer interações com o álcool e manter suas interações com outras moléculas de água, as interações com a água são energeticamente muito mais favoráveis.
Finalmentes
É muito comum, quando se discute o tópico das interações moleculares, se comparar a força dessas interações. Já demonstrar essa comparação diretamente, com experimentos, é algo que me parece muito mais interessante. Este experimento pode despertar uma grande curiosidade nos alunos, que pode ser aproveitada em discussões muito ricas sobre a Química deste fenômeno.

